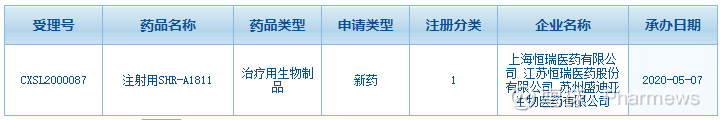
2020年5月7日,国家药品监督管理局药品审评中心公示,已受理恒瑞医药与盛迪亚生物医药提交的一类生物药SHR-A1811临床申请。
该产品具体靶点机制尚未披露,但最新公示临床表明,该产品用于HER2表达/突变的晚期恶性实体瘤(NCT04446260)——《A Phase 1 Multi-Country, Multi-Center, Open-Label Study to Evaluate the Safety, Tolerability, Pharmacokinetics and Efficacy of SHR-A1811 in HER2 Expressing or Mutated Advanced Malignant Solid Tumor Subjects》。
该产品具体靶点机制尚未披露,但最新公示临床表明,该产品用于HER2表达/突变的晚期恶性实体瘤(NCT04446260)——《A Phase 1 Multi-Country, Multi-Center, Open-Label Study to Evaluate the Safety, Tolerability, Pharmacokinetics and Efficacy of SHR-A1811 in HER2 Expressing or Mutated Advanced Malignant Solid Tumor Subjects》。
该临床预计招募226位受试者,计划于7月份开启。
————————
2020年8月更新——恒瑞官方公告中如下描述该HER2-ADC:
注射用 SHR-A1811 可通过与 HER2 表达的肿瘤细胞结合并内吞,在肿瘤细胞溶酶体内通过蛋白酶剪切释放毒素,诱导细胞周期阻滞从而诱导肿瘤细胞凋亡,拟用于治疗 HER2 表达或突变的晚期实体瘤。
————————
2021年3月更新:在2020年8月启动针对HER2表达的胃癌/胃食管连接部腺癌以及结直肠癌等消化道肿瘤(NCT04513223)后,2021年3月26日,恒瑞公布SHR-A1811针对HER2表达、扩增或突变的晚期非小细胞肺癌(NCT04818333)临床,预计招募120人,第一部分包括了”four pre-defined dose regimens“,而就在十天前(即2021年3月26日),科伦博泰刚刚公示其HER2-ADC用于非小细胞肺癌的I/II期临床。
评论